martes, 1 de octubre de 2019
RECONOCIMIENTO DE GLÚCIDOS
a) Informe escrito.
b) Powerpoint con descripción con imágenes de las prácticas.
c) Un vídeo explicativo.
La 1ª práctica va a consistir en distinguir azúcares reductores de los que no los son, mediante la Reacción de Fehling (diseñada por el químico alemán von Fehling a mediados del XIX).
Para ello, vamos a utilizar algunos monosacáridos y disacáridos.
TODOS LOS MONOSACÁRIDOS CÍCLICOS SON REDUCTORES (reducen al Cu2+ del licor de Fehling) porque tienen un grupo -OH hemiacetálico (p.ej. glucosa) o hemicetálico (p.ej. fructosa) libres, con carácter reductor.
LOS DISACÁRIDOS PUEDEN SERLO O NO, dependiendo de si en el enlace glucosídico han intervenido uno (reductor) o dos (no reductor) -OH hemi(a)cetálicos, ya que en el primer caso conserva un -OH hemi(a)cetálico libre y en el segundo ninguno.
Trata de predecir, según su estructura, si los siguientes disacáridos serán o no reductores:
a) Sacarosa (Glu+Fru)
b) Lactosa (Glu+Gal)
c) Maltosa (Glu+Glu).
Ahora comprueba si habías acertado, haciendo la prueba de Fehling.
Si calentamos la sacarosa con HCl al 10% y calentamos, se hidroliza (se rompe el enlace glucosídico). Predice si ahora la disolución resultante será Fehling+ o Fehling-. Comprueba si habías acertado haciendo la prueba.
LOS POLISACÁRIDOS, como el almidón, NO SON REDUCTORES, porque aunque conserven un grupo -OH hemi(a)cetálico en un extremo libre, puede ser uno entre más de mil unidades de glucosa, y además puede estar "escondido", de modo que no está accesible para reducir al Cu2+.
¿El almidón dará la reacción de Fehling? Predice el resultado y compruébalo. ¿Y si lo hidrolizamos?
Ahora bien, el almidón se puede distinguir mediante la prueba del lugol (KI en iodo), ya que lo tiñe intensamente de azul-morado. No se trata de una reacción química, al contrario que la prueba de Fehling, sino de una pura reacción física en la que el almidón cambia de color al introducirse entre sus unidades de glucosa los iones de ioduro. Compruébalo.
jueves, 2 de mayo de 2019
miércoles, 1 de mayo de 2019
miércoles, 10 de abril de 2019
REINO MONERAS
Son procariotas con mp de con AG y PC de peptidoglucano.
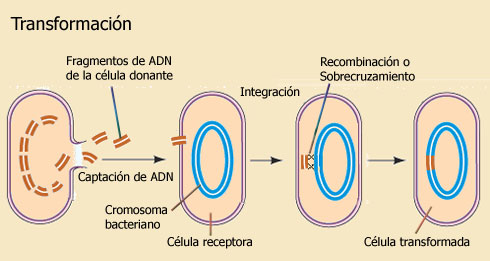
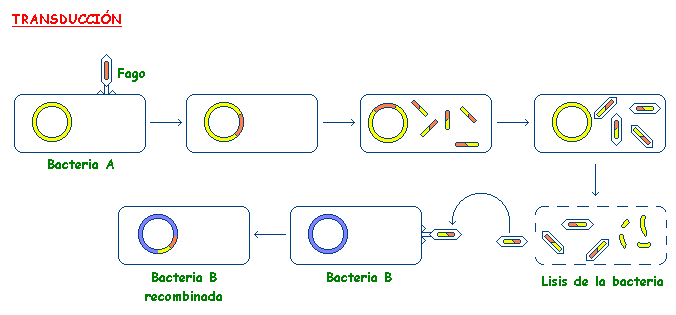
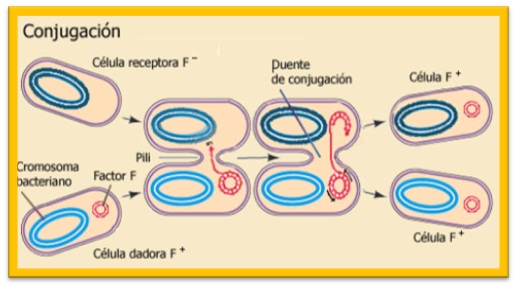
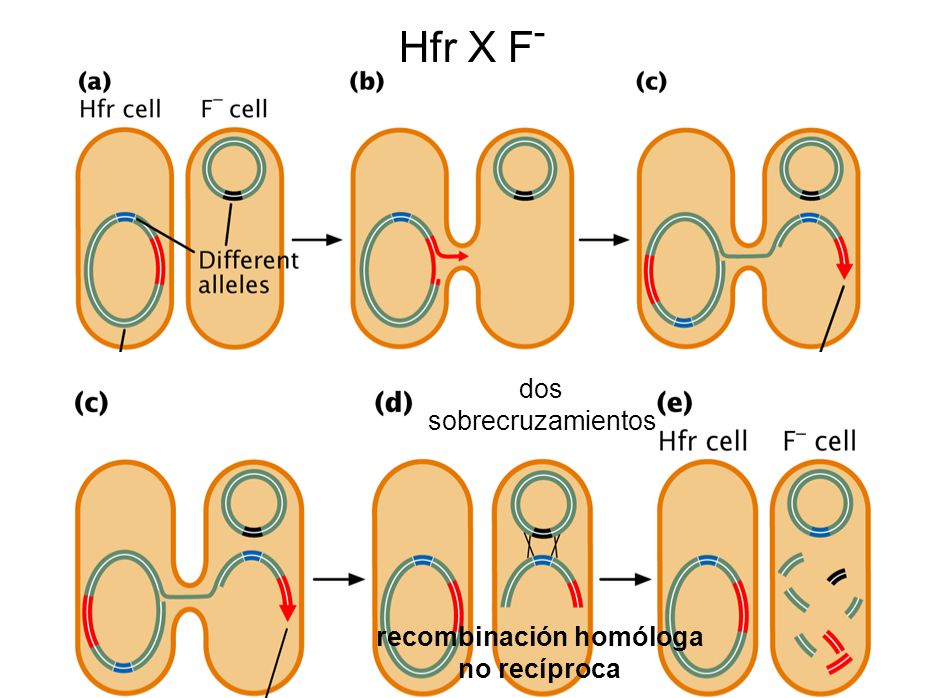
Reproducción bacteriana y mecanismos parasexuales
Las bacterias tienen reproducción asexual por bipartición (fisión binaria), de modo que se reproducen exponencialmente (una colonia de E. coli duplica su tamaño en condiciones óptimas cada 20 minutos), pero como la reproducción asexual sólo permite aumento de la variabilidad genética por mutación , las bacterias han adoptado unos mecanismos para aumentarla, que en cierto modo recuerdan a las exualidad, pero no es un modo de reproducción sexual.
martes, 5 de febrero de 2019
lunes, 28 de enero de 2019
Unidad 8. El catabolismo
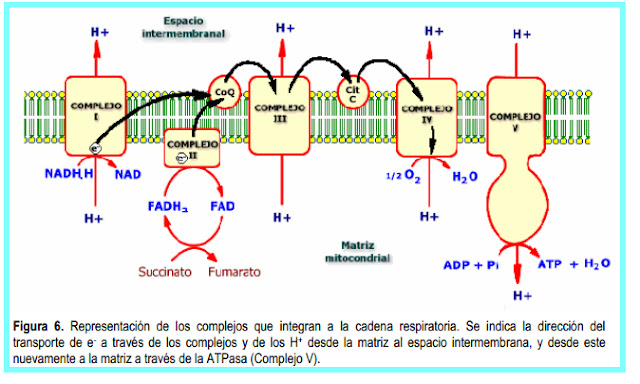
Por cada 4H+ translocados se va a producir un ATP en el complejo V o ATPasa (ATP -Sintasa); de modo que como el NADH mitocondrial cede sus electrones al complejo I, va a originar 3ATP. Como el FADH2 lo hace después del complejo I, solo va a originar 2 ATP. Respecto al NADH citosólico, el de la glucólisis, depende qué lanzadera utilice para entrar en la matriz (necesita una lanzadera ya que las membranas mitocondriales son impermeable al NADH). Si utilizan la lanzadera del glicerol-3-P, que transfiere los electrones al FAD, se originan 2 ATP (esto ocurre en las células musculares y cerebrales, ya que permiten una mayor velocidad en la fosforilación oxidativa, pero solo van a rendir 36 ATP/glucosa). Si utilizan para entrar la lanzadera alternativa, la del malato, su rendimiento energético es mayor, ya que los electrones del NADH son transferidos al Complejo I, originando 3 ATP, y rindiendo 38 ATP/glucosa. Esto ocurre en las células del músculo cardíaco, renales y hepáticas).
- V. ATPasa, ATP-SINTASA O ATP-SINTETASA: La hipótesis del acoplamiento quimiosmótico, lo que el valió el Premio Nobel de Química a Peter D. Mitchell, explica que la cadena de transporte de electrones y la fosforilación oxidativa están acopladas por el gradiente de protones. El flujo de protones crea un gradiente de pH y un gradiente electroquímico. Este gradiente de protones es usado por el complejo V o ATP sintasa para formar ATP vía la fosforilación oxidativa. La ATP sintasa actúa como un canal de iones que "devuelve" los protones a la matriz mitocondrial, de modo que cada 3H+ que se unen a la ATPasa para pasar a la matriz, la enzima gira, a modo de turbina, convirtiendo la energía cinética liberada al rotar en energía química formando ATP a partir de ADP y Pi.
- La ATP sintasa forman ATP utilizando la energía libre procedente del gradiente de protones, utilizando el hecho de que los protones tienden a volver al interior del orgánulo, y sólo pueden hacerlo a través de la ATP sintasa, ya que la membrana interna es impermeable a los protones.
- Cuando los protones son bombeados fuera de la matriz, el espacio intermembrana se convierte en más ácido y con mayor carga positiva que en la matriz. La matriz es más básica y más negativa. Mitchell utilizó el término “quimiosmótico” para describir las reacciones enzimáticas en las que intervienen, simultáneamente, una reacción química y un proceso de transporte.
- Esta enzima está formada por dos complejos principales. Uno, que atraviesa la membrana mitocondrial interna
- . El otro, que sobresale de la membrana, se llama F1 .
El acoplamiento con la fosforilación oxidativa es un paso clave en la producción de ATP. Sin embargo, en ciertas ocasiones desacoplarlo puede tener usos biológicos. En la membrana interna mitocondrial de los tejidos adiposos marrones existe una gran cantidad de termogenina, que es una proteína desacopladora, que actúa como una vía alternativa para el regreso de los protones a la matriz. Esto resulta en consumo de la energía en termogénesis en vez de utilizarse para la producción de ATP. Esto puede ser útil para generar calor cuando sea necesario, por ejemplo en invierno o durante la hibernación de ciertos animales.
También se conocen desacoplantes sintéticos como el caso del 2,4-dinitrofenol, que se ha usado como pesticida, debido a su alta toxicidad.
CALCULA REL RENDIMIENTO ENERGÉTICO (Nº DE ATP) A PARTIR DE UNA GLUCOSA OXIDADA TOTALMENTE CON EL CATABOLISMO AEROBIO
CATABOLISMO DE LOS TRIGLICÉRIDOS
El glicerol entra en la glucólisis, mientras que los ácidos grasos entran en el Ciclo de Krebs, a través de la beta-oxidación, que va escindiendo los A.G. en grupos acetilo que se unen al CoA, dando moléculas de AcCoA. Cada A.G. genera muchos más ATP que una glucosa (p.ej. el ácido palmítico produce 130 ATP).
CATABOLISMO DE LOS AMINOÁCIDOS
Los aa sufren una desaminación, dando lugar a cetoácidos, que entran en el Ciclo de Krebs, y amoníaco, que en los mamíferos, mediante el ciclo de la urea, se convierten en esta molécula menos tóxica, que se lleva a los riñones para su eliminación.


